2026年3月30日、厚生労働省から「治験等に係る情報提供の取扱いについて」(医薬監麻発0330第1号)が発出されました。治験をはじめとする未承認医薬品の臨床試験に関する情報提供が、薬機法(医薬品医療機器等法)上の広告規制にどう当たるかを整理し直した通知です。同日、企業向けQ&Aおよび患者団体向けQ&Aも合わせて発出されています。
一見すると専門的な行政通知に見えますが、臨床開発・製薬・CRO(医薬品開発受託機関)の実務担当者にとって影響は小さくありません。本通知によって、治験参加者のリクルートメント(参加者募集)やエンロールメント(試験への組み入れ)を取り巻く情報環境の前提が変わり始めるからです。
この記事では、従来の規制構造と実務上の課題を整理した上で、今回の通知で何がどう変わったのかを、CRA視点から解説します。
この通知が出た背景:規制改革実施計画から始まる変化
日本における治験情報の発信は、長らく非常に限定的な範囲にとどまってきました。その背景には、薬機法第68条に基づく未承認医薬品の広告規制があります。治験薬は承認前の医薬品であるため、この規制の対象となります。
制度上の出発点はシンプルですが、実務では「その情報提供が広告に当たるかどうか」という判断が一貫して難しい状況でした。判断の曖昧さは企業側の情報発信の抑制につながり、結果として患者が治験について調べようとしても必要な情報が得られないという状況を生み出していました。
この問題は政策的にも認識されており、規制改革実施計画において「治験に係る広告規制の見直し」が明示されています(規制改革WG資料)。
広告規制の基本構造:なぜ治験情報は出しにくかったのか
広告該当性を決める「3要件」
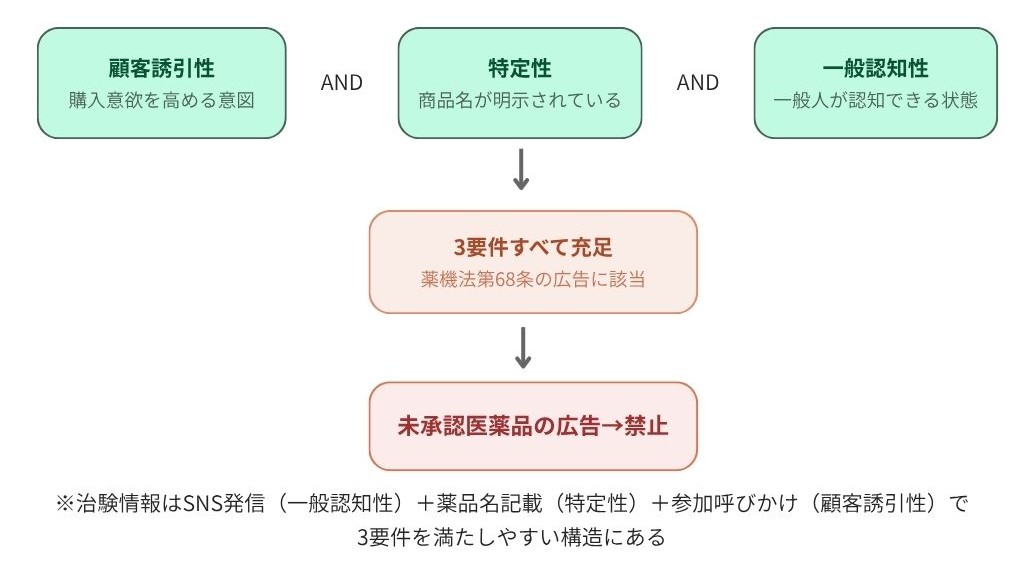
薬機法上の広告に該当するかどうかは、平成10年の厚生省通知(医薬監第148号)以来、以下の3要件により判断されています。
- 顧客誘引性(顧客の行動を促す意図)
- 特定性(特定の医薬品が識別できる)
- 一般認知性(不特定多数が認知可能)
この3要件をすべて満たす場合、広告に該当します。
令和5年(2023年)にも前身となる通知(薬生監麻発0124第1号)が出されていましたが、「情報を求める者に限定する」などの文言が抽象的で、実務への落とし込みが難しい状態でした。URLの掲載方法やSNSへの投稿など、具体的なケースにどう対応すべきかが不明確なまま現場に委ねられていました。
患者団体にとっては特に問題が大きいものでした。製薬企業とは異なり、中立的な立場で情報を提供しようとしても、「顧客誘引性があるかどうか」の判断が難しく、リスク回避のために情報発信そのものを控えざるを得ない状況が続いていました。
今回の新通知は、このような曖昧さを解消することを主たる目的としており、令和5年通知はこれにより廃止されています。背景には、令和7年6月の閣議決定「規制改革実施計画」において、「治験に係る広告規制の見直し」が明示的に盛り込まれたことがあります。
「特定性を避ける」という苦肉の策とその限界
こうした状況への対応として、実務では「治験薬名を記載しない」という運用が慣習的に行われてきました。特定性がなければ広告の3要件を満たさない、という論理によるものです。
しかしこの運用は、患者視点からは本質的な問題を残します。治験薬名が伏せられた状態では、患者は自分の病気・状況に合った治験かどうかを判断できません。結果として、「情報は存在するが、患者が必要な形で届いていない」という情報非対称の状態が固定化されていました。
PRO(患者リクルートメント組織)はどう乗り越えてきたか
段階的開示による「能動性」の設計
こうした規制環境のなかで、実務的な解決策として機能してきたのがPRO(Patient Recruitment Organization)、臨床試験の参加者リクルートメントを専門とする事業者群です。日本では「パネル」と呼ばれることもあります。
PROの基本は、「情報を段階的に開示する」構造にあります。
たとえば最初に「糖尿病の治験募集中」といった疾患名レベルの抽象的な募集が出ます。この段階では治験薬名は含まれず、広告規制上の「特定性」を満たさない設計になっています。
この後も同様に構造を分解すると、以下のように整理できます。
- Step 1:抽象情報の公開
疾患名レベルの募集情報のみを提示(特定性なし) - Step 2:登録・問い合わせ
ユーザーが自ら情報取得のアクションを起こす(能動性の成立) - Step 3:条件マッチング
適格性の確認・スクリーニング - Step 4:詳細情報の提示
該当試験のみ、治験薬名を含む情報を開示(特定性あり)
※この段階でユーザーは「能動的に情報を求めた者」と整理され、顧客誘引性の観点で広告該当性は低く評価されやすくなります。
PROはこのような段階設計により、「自ら情報を取りに来た人にのみ詳細を提示する」状態を作り、広告規制との整合を図ってきました。
このモデルの課題:登録ハードルと情報アクセス性の壁
PROのアプローチは規制上の問題を巧みに回避してきましたが、ユーザー体験の観点では一定の制約を抱えていました。
個人情報の入力・登録というハードルが、情報アクセスを実質的に絞り込みます。法規制上、登録自体が義務付けられているわけではありませんが、「能動的に求めた者」であることを担保する実務的な手段として、登録という形式を取らざるを得ませんでした。
登録を前提とする構造は、患者にとって心理的・実務的な障壁となります。適格性基準や来院スケジュールといった重要情報が登録後でないと見えない点も、意思決定の妨げになります。
結果として、「アクセス制御」と「情報提供」のトレードオフが解消されないままでした。
新通知の核心:何が、どう変わったか
令和5年通知(旧)
-
参加者募集
「情報を求めるものに限定」という抽象的な条件みの。SNSや広告媒体での利用は明確に認められず
-
試験結果等の情報提供
要件・構造要件の定めなし。実務判断が困難で、ほぼ発信されていない状況。 -
患者団体
広告該当性の個別判断が困難。情報提供を自主的に控える状況が続く。
-
SNS・URL掲載
具体的なルールなし。現場での判断が不可能な状態。
新通知(2026年3月)
-
参加者募集
jRCT登録済み・同意文書の範囲内・実施期間中・留意事項記載の4要件を満たせば、治験薬名記載も含めSNS・雑誌等の媒体を問わず発信可能に。 -
試験結果等の情報提供
「表紙ページ構造」(個別ページへの直接リンク禁止・リダイレクト推奨)を設ければ、jRCT情報・レイサマリーの提供が可能に。 -
患者団体
製薬企業から独立した中立団体が、新通知準拠の情報を改変せず会員等に提供する場合は明確に広告に該当しないと整理。 -
SNS・URL掲載
参加者募集ページURL・表紙ページURLのSNS掲載は明示的に許容。個別ページへの直接リンクは広告リスクあり。
参加者募集:条件付きでSNS・各種媒体も解禁
今回の新通知では、参加者募集を目的とした情報提供について、以下の4要件を満たす場合は「顧客誘引性がない」と明確に整理されました。治験薬名等の特定性を含む情報であっても、広告に該当しないとされています。
-
jRCT(臨床研究等提出・公開システム)に試験が登録済みであること
-
情報の内容が当該試験の同意説明文書の範囲内に収まること
-
情報提供が試験の実施期間中に限定されること(治験の場合は治験届提出日以降)
-
「治験薬の有効性・安全性は検証されたものではない」旨の留意事項を分かりやすく記載すること
要件を満たす場合、この情報提供のためのウェブページURLを、製薬企業のウェブサイト・新聞・雑誌・SNS投稿・動画配信等で紹介することが可能とされました。SNSの文字数制限等でURLのみの掲載となる場合は、リンク先のページに留意事項が記載されていれば、投稿本文での省略も許容されます。
参加者募集という目的が明確な情報提供については、媒体を問わず広告に該当しないと整理されたことが、今回の通知における最大のポイントの一つです。
試験結果等の情報提供:「表紙ページ構造」による制御
参加者募集以外の情報提供、たとえば試験結果のレイサマリー(一般市民向けに平易に記述した要約)やjRCT等の登録情報を患者向けに提供する場合については、引き続き慎重な扱いが求められます。
この類型の情報提供を広告に該当しないと判断するために、新通知が要件として定めたのが「表紙ページ構造」です。
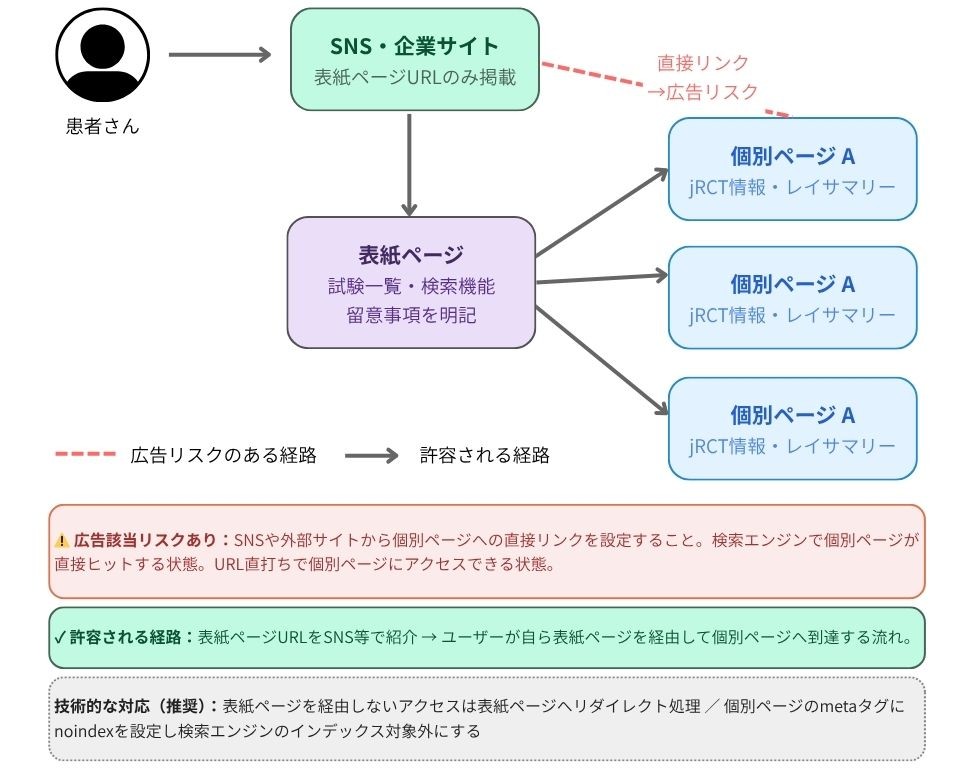
個別の治験に関する詳細情報(個別ページ)は独立したページとして設け、そのページへの直接リンクは設定しません。代わりに、個別ページの一覧や検索機能を持つ別ページ(表紙ページ)を経由する構造とすることが求められます。通知では、この構造をより確実に担保するため、表紙ページを経由しないアクセスは表紙ページにリダイレクトさせる処理や、個別ページのメタデータを検索エンジンのインデックス対象外(noindex)に設定することが「望ましい」とも記載されています。
個別ページで提供できる情報の範囲は、jRCT等の公的データベースに登録された情報、または臨床試験の結果のレイサマリー(PPI JAPANの作成指針や欧州委員会のGood Lay Summary Practice等に準拠したもの)に限定されます。有効性・安全性について患者の期待を煽るような表現は引き続き厳に慎む必要があります。
本質的な変化:「内容」から「構造」へ
今回の通知の本質をひと言で言えば、広告該当性の判断が「内容」から「導線・アクセス構造」へと軸足を移したことにあります。情報の内容が問われることに変わりはありませんが、加えて「どのような経路でユーザーがその情報に到達するか」が、規制の判断基準として明示的に位置づけられました。
すなわち、規制の焦点が「何を書くか」から「どう見せるか」へ移行しました。
PROが人的・運用的なプロセス(登録フロー)によって能動性を担保していたのに対し、新通知の求める構造はサイト設計・導線設計によって同様の効果を実現しようとするものです。制御主体が「人の判断・運用」から「UIとアーキテクチャ」に移行したと整理することができます。
実務での読み方:SNS・Webサイト・患者団体のケース別整理
SNS運用の整理
SNSはプッシュ型の媒体であり、投稿は原則として不特定多数に届きます。そのため、SNS上で試験結果の要約や有効性に関する情報を発信することは、今回の通知以降も広告に該当するリスクが高い状況です。
一方で、参加者募集のためのウェブページのURLをSNSで紹介することは、新通知上明示的に許容されています。また、表紙ページのURLをSNSで紹介することも広告には当たらないとされました。
-
参加者募集ページURLの紹介
「2型糖尿病の治験参加者を募集しています。詳細はこちら(URL)」 -
表紙ページURLの中立的な紹介
「当社の臨床試験情報ページを更新しました(表紙ページURL)」 -
試験名のみ言及(内容に触れない)
「○○試験のレイサマリーが掲載されました(表紙ページURL)」 -
jRCT等の公的DBトップページの紹介
「jRCTで治験情報を検索できます(jRCTトップURL)」
-
個別ページへの直接リンク
「○○試験の結果はこちら(個別ページの直接URL)」 -
有効性・安全性の結果を要約・抜粋
「○○試験で対照薬より有効性が高い結果が示されました」 -
個別ページ内容の抜粋をSNSに掲載
「今回の試験では、○○mg投与群で改善が確認されました」 -
承認済み薬の情報から個別ページへ誘導
承認薬の情報ページ内に個別ページへのリンクを設置する行為
※上記はQ&Aを参照した実務的な整理です。個別案件の判断は所管当局または法律の専門家にご相談ください。
整理すると、SNSは「入口の案内」として使い、情報の実体は構造化されたWebサイト上で見せるという役割分担が実務上の基本となります。
Webサイト設計:表紙ページ構造の具体像
製薬企業や試験依頼者が試験結果等を患者向けに公開する場合、サイト設計の観点から以下の要素が求められます。
- 治験・臨床試験の情報を一覧できる表紙ページを設置すること
- 個別試験の詳細ページへは表紙ページのみからアクセスできる構造にすること
- 個別ページへの直接URLリンクを外部に設定しないこと
- 表紙ページを経由しない直接アクセスについてはリダイレクト処理を行うこと(推奨)
- 個別ページのメタデータをnoindexに設定すること(推奨)
コンプライアンス対応がサイトアーキテクチャの問題になるという点は、臨床開発部門とデジタル部門の連携を不可欠にします。
患者団体等の扱い:中立性と利益相反管理が前提
患者団体向けQ&Aで整理されたのは、患者団体等が治験情報を提供する場合の判断基準です。製薬企業から独立した中立的立場にある団体が、新通知に則って製薬企業から提供された情報を内容を改変せずに会員等に提供する場合は、広告に該当しないと判断して差し支えないとされました。
ここでの「会員等」の要件は緩やかに解釈されており、正式な会員登録だけでなく、情報提供の依頼をした患者・家族や、会合への参加申込みをした者も含まれます。ただし、製薬企業との利益相反の管理が適切になされていることが前提条件として求められる点には注意が必要です。
患者団体が独自に作成した情報については、新通知の保護の対象外となり、個別に広告該当性を判断する必要があります。情報の正確性を担保する観点からも、製薬企業から入手した情報をそのまま提供することが通知上推奨されています。
海外との比較:米国はなぜ「オープン」に見えるのか
米国では、臨床試験情報は比較的オープンに公開されており、企業サイトやSNSを通じた情報発信も日本ほど制限されていません。この違いは規制の哲学の差に起因します。
米国の規制は主に「情報の内容が適切か」という観点から判断され、情報へのアクセス経路や導線設計そのものを規制の要件としていません。一方、日本では今回の新通知により、アクセス経路の設計が広告該当性の判断要素として明示的に組み込まれました。
日本が「構造で制御する」アプローチを採ったことは、情報の安全性への配慮という観点では理解できます。未承認薬への患者の過度な期待を防ぐという目的は、規制の根拠として合理的です。ただし、その結果として技術的な実装の複雑さが増し、中小規模の組織や患者団体には実務的なハードルが生じる点は課題として残ります。
日本の新薬開発への影響:エンロールメント改善とドラッグロス問題
今回の通知が臨床開発の実務に与える最も重要な影響は、患者リクルートメント・エンロールメントのプロセスが変わりうる点にあります。
日本では、グローバル試験への参加症例の集積に時間がかかることが長年の課題として指摘されてきました。エンロールメントの遅延は試験のタイムライン全体に影響し、最終的には承認の遅れ、すなわち患者が新薬にアクセスできるまでの期間の長期化につながります。これはドラッグラグ・ドラッグロスの一因として複数の報告で指摘されている問題です。
情報発信の制約が緩和され、患者が自ら治験を調べ、参加を検討できる環境が整いつつあるとすれば、エンロールメント改善への寄与が期待されます。特に、SNSや製薬企業サイトを通じた参加者募集情報の発信が正面から認められたことで、PROへの依存を一定程度減らしながら自社でのリクルートメント活動を強化できる可能性があります。
また、PPI(Patient and Public Involvement:患者・市民参画)の文脈でも変化が見込まれます。治験に関する情報が可視化されることで、患者が「試験を知らなかった」という状況が減れば、選択肢としての治験参加が現実的になります。これはグローバル試験における日本サイトの競争力にも関係する話です。
一方で、規制の詳細を踏まえた正確な情報発信ができるかどうかは、各社の体制に依存します。臨床開発の専門性とデジタルマーケティングの知見を組み合わせた実務能力がより重要になっており、CRO・PRO・ヘルステック企業などの新たな役割が生まれる余地もあります。
おわりに:「出すな」から「設計して出す」時代へ
今回の通知を一言で表現すれば、「出すな」から「適切に設計すれば出せる」への転換です。しかしそれは、情報発信の全面的な自由化ではありません。「何を書くか」と「どう見せるか(導線・構造)」の両方を制御することが、コンプライアンスの要件となりました。
治験薬の有効性・安全性はまだ検証されていないという大前提は変わりません。患者が誤った期待を抱かないための留意事項の記載義務も、参加者募集・結果提供のいずれにおいても課せられています。新通知が緩和したのは「発信の可否」であり、「発信の責任」が軽くなったわけではありません。
実務的には、Webサイトの構造設計、SEO対策との整合、リダイレクト実装、SNS運用ポリシーの見直しなど、新たな課題も立ち上がっています。Clinical×Digitalという横断的なスキルが、これからの臨床開発の実務では求められていきます。
【免責事項】
本記事は厚生労働省が発出した一次資料(医薬監麻発0330第1号通知・関連Q&A2件)に基づき執筆した実務的な解説であり、筆者個人の見解を含みます。個別案件の法的判断については、所管当局または法律の専門家に必ずご相談ください。通知の詳細は厚生労働省ウェブサイトでご確認ください。
【出典】
- 治験等に係る情報提供の取扱いについて(令和8年3月30日付け医薬監麻発 0330 第1号 厚生労働省医薬局監視指導・麻薬対策課長通知)
- 治験等に係る情報提供の取扱いに関するQ&Aについて(令和8年3月30日付け事務連絡 厚生労働省医薬局監視指導・麻薬対策課)
- 患者団体等による治験等に係る情報提供に関するQ&Aについて(令和8年3月30日付け事務連絡 厚生労働省医薬局監視指導・麻薬対策課)
- 治験等に係る情報提供の取扱いについて(令和8年3月26日 第45回 臨床研究部会 厚生労働省 医薬局監視指導・麻薬対策課)
- 令和7年3月6日 健康・医療・介護WG 厚生労働省提出資料「治験に係る広告規制について」
- 治験に係る情報提供の取扱いについて(令和5年1月24日付け薬生監麻発 0124 第1号厚生労働省医薬・生活衛生局監視指導・麻薬対策課長通知)
- 患者及び一般市民を対象とした治験に係る情報提供の要領 第3版(令和5年11月 日本製薬工業協会医薬品評価委員会)
- 医薬品等の広告規制について(厚生労働省)




コメント