「治験」「臨床研究」「特定臨床研究」――言葉は知っていても、関係性をすっと説明できる人は意外と少ないものです。制度の全体像を一度地図として整理しておくと、現場で新しい言葉に出会うたびに迷わなくなります。
-
治験・臨床研究・特定臨床研究の包含関係と違い
-
観察研究・介入研究の違いと、侵襲との関係
-
GCP省令・GPSP省令・臨床研究法それぞれの役割
-
制度全体を一覧表で整理したまとめ
CRC・CRA・学生・就活生、および治験に関心のある患者さん・ご家族
すべての出発点――「臨床研究」とは何か
まず、一番大きな枠組みから確認します。
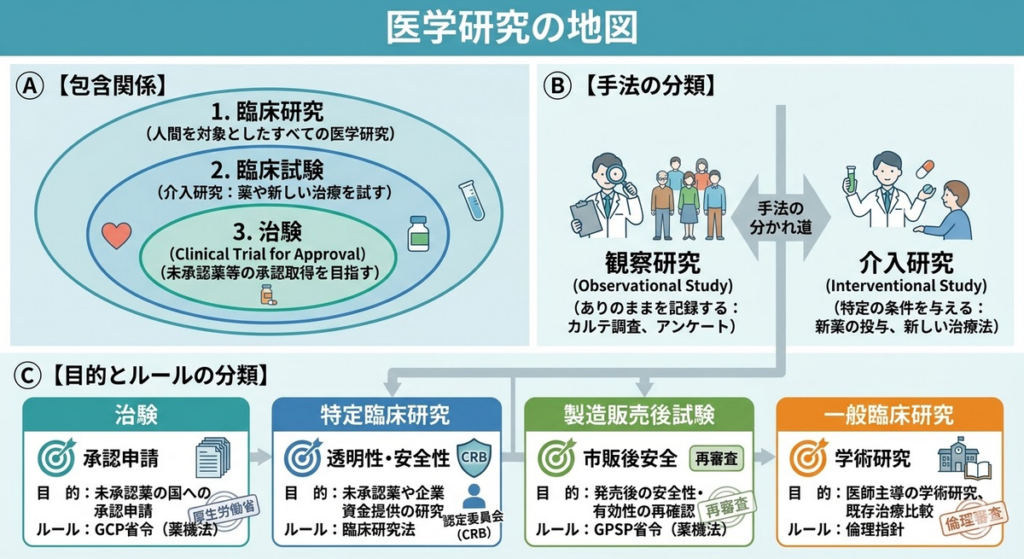
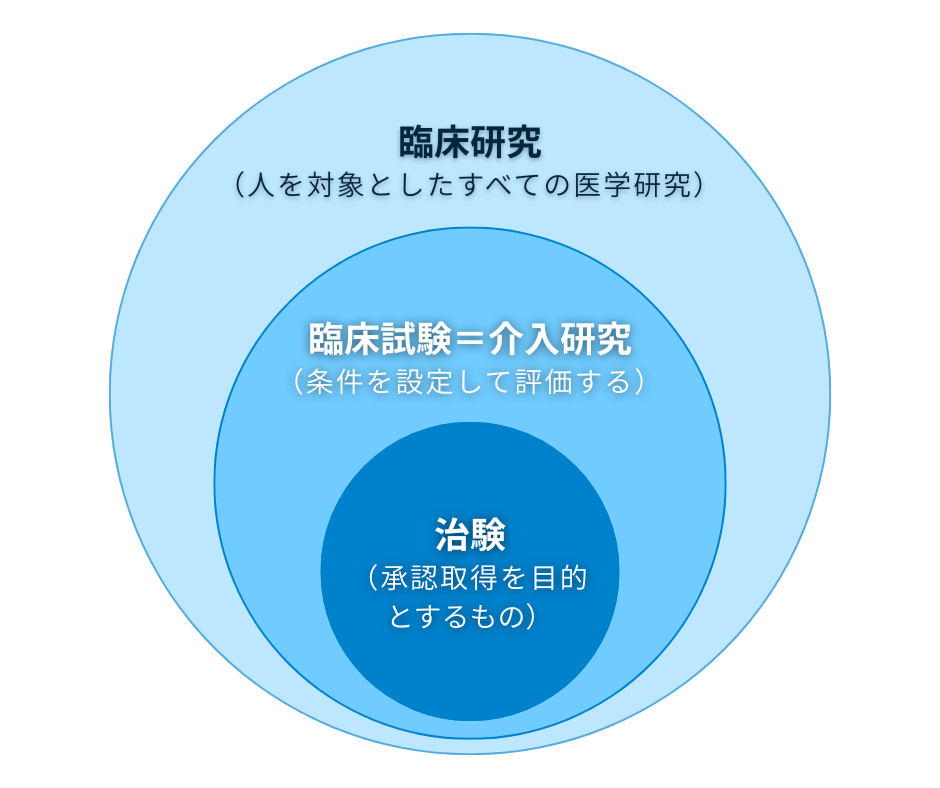
臨床研究とは、人(患者さんや健康な方)を対象に、病気の原因解明・予防・診断・治療法の改善を目指して行われる、あらゆる学術的な活動のことです。「治験」も「特定臨床研究」も、すべてこの「臨床研究」という大きな傘の中に含まれます。つまり、治験は臨床研究の一種です。この包含関係を最初に押さえておくと、以降の話がぐっとわかりやすくなります。
研究手法による分類――「観察」か「介入」か
臨床研究は、研究者が対象者にどう関わるかによって、大きく2つに分けられます。以降の説明は、A〜Cの3つのブロックに分かれた全体図の構造に沿って進みます。
観察研究
研究者が患者さんに何かを「させる」のではなく、医師が自身の判断で行った診療の結果や、患者さんの現在の状態を「記録・分析する」研究です。
-
薬の種類や量は医師の裁量に委ねられ、研究者が指定しません
-
過去のカルテを遡って調べる後ろ向き研究も、ここに含まれます
具体例:「血圧の薬を服用している100人の、5年後の健康状態を追跡調査する」

野鳥観察に例えるなら、双眼鏡で眺めるだけで、鳥の生活には一切手を触れないイメージです。
介入研究(=臨床試験)
研究の目的を達成するために、研究者が患者さんに対して意図的なアクション(介入)を加える研究です。
「臨床試験」は「介入研究」とほぼ同義で使われる言葉で、「研究として条件を設定し、治療や検査を意図的に組み込んで評価する」という意味合いを持ちます。治験はこの臨床試験の中に含まれる、特定の目的(承認取得)を持つものです。
介入研究の特徴として、「AグループはX薬を、BグループはY薬を投与する」といった割り付けが存在します。未承認薬はもちろん、すでに承認された薬であっても「この用量で試す」と研究者が設定すれば「介入」になります。
具体例:「新薬Aと既存薬Bをランダムに割り振り、効果の差を比較する」
なぜ「ランダムに割り振る」のか
介入研究では、しばしばランダム化(無作為割り付け)という手法が使われます。「どちらのグループに入るかを、くじ引きのようにランダムに決める」というものです。
これは、「この薬が効いた」という結果が、薬そのものの効果なのか、たまたまその患者さんの体質によるものなのかを、できる限り切り分けるためです。
さらに進んだ手法として盲検化(もうけんか)もあります。参加者が「自分が本物の薬を飲んでいるのか、偽薬(プラセボ)を飲んでいるのかを知らない状態」にすることで、思い込みによるバイアスを排除します。医師側も知らない状態にする「二重盲検」は、最も厳格な試験デザインのひとつです。
「介入」と「侵襲」は別の軸
観察研究か介入研究かを考えるとき、もう一つ混乱しやすいポイントがあります。それが侵襲(しんしゅう)との違いです。
侵襲とは、採血・生検・投薬など、身体に何らかの負担や影響を与える行為を指します。
現場でよく出る疑問として、「疾患の経過観察で採血回数が多い研究は、介入研究になるのか」というものがあります。結論から言えば、採血の回数が多くても、研究者が割り付けや治療上の指示を行っていなければ介入研究にはなりません。
2つは以下のように、独立した別の軸の話です。
| 侵襲あり | 侵襲なし | |
|---|---|---|
| 介入研究 | 新薬投与+採血 | 食事指導の割り付け(採血なし) |
| 観察研究 | 経過観察中の定期採血 | アンケート調査 |
「介入かどうか」は研究者が治療や条件を意図的に操作しているかどうか、「侵襲かどうか」は身体への負担があるかどうか——この2つは独立した問いです。
なお、侵襲の有無は倫理審査における手続きの重さに影響します。倫理指針では侵襲を「軽微な侵襲」とそれ以外に区分しており、侵襲を伴う観察研究であっても、その程度に応じて同意取得の方法が変わります。介入か否かと侵襲の程度は、別々に考える必要があります。
なぜ「介入があるかどうか」が重要なのか
介入研究では、通常の診療には存在しない未知のリスクや追加の負担が参加者(患者さん)に生じます。だからこそ、観察研究よりも厳しい倫理審査と、より丁寧な説明と同意(インフォームド・コンセント)が法律や指針によって義務付けられています。
インフォームド・コンセント(IC)とは、研究の目的・方法・期待される効果・起こりうるリスクについて十分な説明を受け、理解したうえで、自分の意思で参加に同意することを指します。同意はいつでも撤回でき、撤回しても不利益を受けないことも保障されています。CRCやCRAにとっては、「ICが義務付けられているのは介入研究だから」という理解の軸を持っておくと、現場での判断がしやすくなります。
薬機法に基づく分類――「治験」と「製造販売後調査」
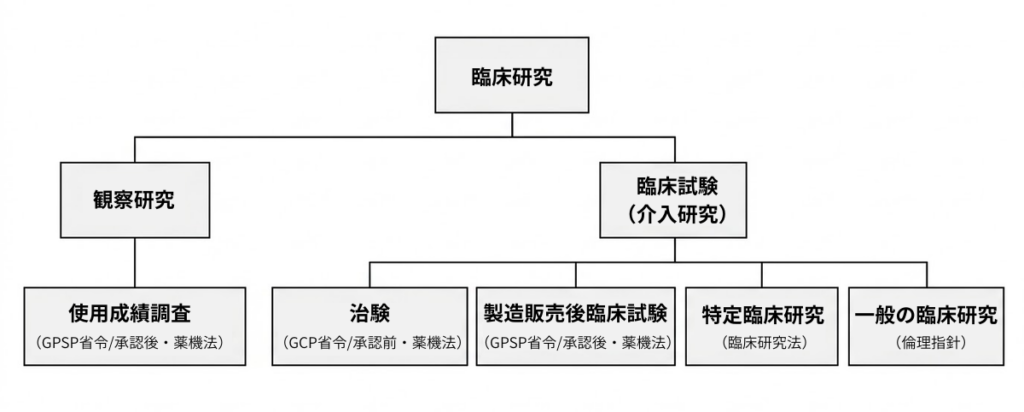
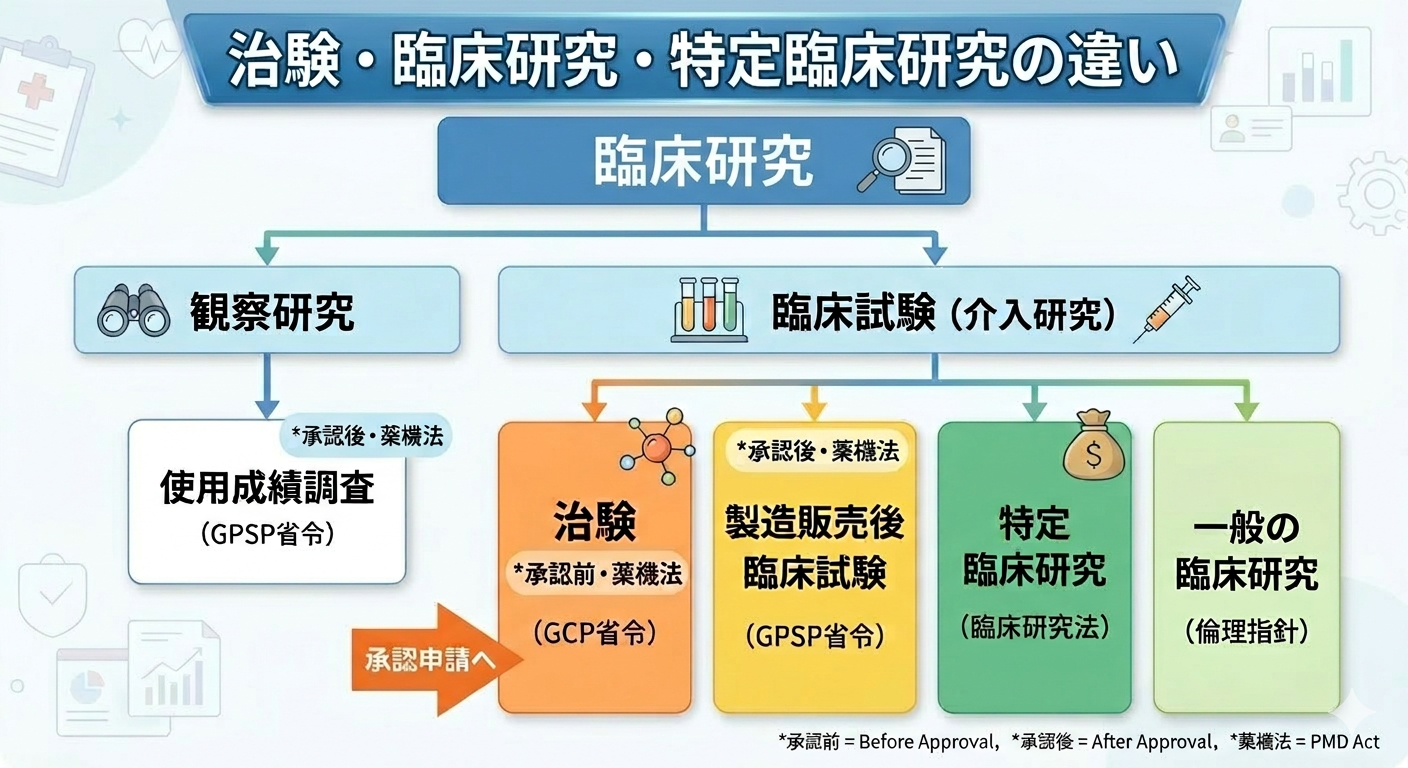
介入研究の中でも、医薬品や医療機器が市場に出る「前」と「後」では、適用されるルールが大きく異なります。どちらも薬機法(医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律)に基づいています。
なお、後述する製造販売後調査(PMS)のうち「使用成績調査」は観察研究に分類されます。介入を伴わないため臨床試験には含まれませんが、薬機法のもとで義務付けられた重要な安全管理プロセスです。
治験(Clinical Trial)
根拠省令:GCP省令(医薬品の臨床試験の実施の基準に関する省令)
治験とは、未承認の薬・医療機器について、国(厚生労働省)から製造販売承認を取得することを目的とした臨床試験です。参加基準が厳しく設定されており、安全性と有効性を初めて体系的に証明するための、最も厳格なプロセスといえます。
治験には第I相〜第III相という段階(フェーズ)があり、それぞれ目的と規模が異なります。
-
第I相: 主に安全性の確認(少人数)
-
第II相: 有効性の探索と用量の検討
-
第III相: 大規模な有効性・安全性の検証
-
第IV相: 承認後も市販後の安全確認を目的として実施されることがある。厳密には治験ではなく、後述する製造販売後臨床試験(GPSP省令)に位置づけられる。
また、治験には企業が主体となる企業治験のほかに、医師自らが依頼者となって実施する医師主導治験があります。どちらもGCP省令が適用されますが、責任の所在や手続きの主体が異なります。後述する特定臨床研究との混同が起きやすいポイントでもあるため、意識しておくと現場での理解が早まります。
製造販売後調査・試験(Post-Marketing Surveillance / PMS)
根拠省令:GPSP省令(医薬品の製造販売後の調査及び試験の実施の基準に関する省令)
薬が承認・発売された後も、実際の医療現場(リアルワールド)での安全性を確認し、国に報告する義務があります。これが製造販売後調査(PMS)です。PMSには大きく2つのルートがあります。
1. 使用成績調査(観察ルート)
医師が通常の診察で処方した結果を、製薬企業が収集・集計する形式です。
-
薬の種類・量・検査タイミングはすべて医師の裁量に委ねられます
-
製薬企業側から「この日にこの検査をしてください」と指示することはありません
-
リアルワールドで「実際にどう使われているか」を広く把握するのに適しています
2. 製造販売後臨床試験(介入ルート)
承認された範囲内で、より厳密にデータを取るために行われる「試験」です。
-
試験計画(プロトコル)に基づき、「〇週目に必ずこの検査をする」といったルールが設定されます
-
条件を揃えることで、特定の有効性・安全性をより精緻に検証できます
| 項目 | 使用成績調査 | 製造販売後臨床試験 |
|---|---|---|
| 研究手法 | 観察研究 | 介入研究(臨床試験) |
| 診察内容 | 医師の裁量(普段通り) | プロトコル通り |
| 検査日程 | 規定なし | 厳密に設定 |
| 主な目的 | 未知の副作用の早期発見 | 特定の有効性・安全性の再確認 |
なぜ発売後も調査・試験が必要なのか
治験は、薬の効果を純粋に確かめるために参加者を厳しく絞り込んで行われます。年齢制限があり、重篤な合併症を持つ方や多くの薬を併用している方は、多くの場合参加できません。参加者数も数百〜数千人規模です。
ところが発売後は、何万・何十万という多様な患者さんが服用します。高齢者、腎機能や肝機能が低下している方、多剤併用の方——治験では見えなかった非常にまれな副作用が、初めて浮かび上がることがあります。
使用成績調査(観察)は「広く浅く、異変を見逃さないためのパトロール」、製造販売後臨床試験(介入)は「絞り込んだ条件で深く掘り下げる追加検証」と理解すると、役割の違いがイメージしやすいかもしれません。

新車開発に例えると次のようなイメージになります。
-
治験:テストコースでプロドライバーが走らせる(完璧な条件でのテスト)
-
使用成績調査:一般道で様々なドライバーが乗る様子をメーカーが見守る
-
製造販売後臨床試験:「雪道での性能をもっと詳しく知りたい」と追加テストを行う
臨床研究法による分類――「特定臨床研究」と「一般の臨床研究」
治験以外の介入研究は、研究のリスクや資金源によって、適用されるルールの「重さ」が変わります。
特定臨床研究
根拠法令:臨床研究法(2018年施行)
以下のいずれかに該当する介入研究が対象です。
-
未承認・適応外の医薬品等を用いる研究(リスクが相対的に高い)
-
製薬企業等から資金提供を受けている研究(企業との利益相反=COIが絡む)
「適応外」について補足します。薬には国から承認された「使っていい病気・使っていい量・使っていい対象年齢」が決まっており、これを効能・効果(適応)と呼びます。この承認された範囲を外れた使い方——たとえば「A病に承認されている薬を、B病の患者さんに使う」こと——を適応外使用といいます。適応外での使用は、薬機法上は医師の裁量の範囲内とされる場合がありますが、それを研究として計画・実施する場合は特定臨床研究の対象となります。
具体例: A大学病院の医師が「既存薬Xは、まだ承認されていない疾患Yにも効くのではないか」という仮説を立て、製薬会社Bから研究資金の提供を受けながら臨床試験を行うケースが該当します。医師が自ら計画・実施する「医師主導」の研究であっても、企業資金が入っていれば対象になります。
臨床研究法は、2017〜2018年ごろに相次いで発覚した研究不正事案(特定の降圧剤に関する論文データ操作など)を背景に制定されました。企業との利益相反や高リスクが絡む研究の透明性と信頼性を確保することが目的で、厚生労働省への届出と、認定臨床研究審査委員会(CRB)による審査が義務付けられています。
一般の臨床研究(非特定臨床研究)
根拠:人を対象とする生命科学・医学系研究に関する倫理指針(いわゆる「倫理指針」)
治験にも特定臨床研究にも該当しない、既存の治療法の比較などを行う学術研究が対象です。法律ではなく「指針」に基づきますが、各施設の倫理審査委員会(IRB)の承認を得たうえで実施されます。医学の進歩を支える、純粋な学術探究の場です。
まとめ:臨床研究の分類と根拠法令・指針
| 区分 | 段階 | 研究手法 | 侵襲の有無 | 主な目的 | 根拠法令・指針 | 主な規制内容 |
|---|---|---|---|---|---|---|
| 治験 | 承認前 | 介入研究 | あり | 新薬・医療機器の製造販売承認取得 | GCP省令(薬機法) | 承認申請資料としての厳格なデータ管理 |
| 使用成績調査 | 承認後 | 観察研究 | なし〜あり | 発売後の安全性確認 | GPSP省令(薬機法) | 再審査のための市販後パトロール |
| 製造販売後臨床試験 | 承認後 | 介入研究 | あり | 発売後の有効性・安全性の精緻な再確認 | GPSP省令(薬機法) | プロトコルに基づく追加検証 |
| 特定臨床研究 | 任意 | 介入研究 | あり | 透明性確保・未承認薬・適応外使用の評価 | 臨床研究法 | 厚労省届出、CRB審査の義務化 |
| 一般の臨床研究 | 任意 | 観察・介入 | なし〜あり | 学術的な真理の探究 | 倫理指針 | 施設内IRB審査 |
制度の全体像は、一度地図として頭に入ってしまえば、現場で新しい言葉に出会うたびに「あの地図のどこにあたるのか」と照らし合わせることができます。この記事がCRC・CRAをはじめ、これから業界に入る学生・就活生の方にとって、手元に置いておける一枚の地図になれば幸いです。
参考・根拠法令
- 医薬品、医療機器等の品質、有効性及び安全性の確保等に関する法律(薬機法)
- 医薬品の臨床試験の実施の基準に関する省令(GCP省令)|e-Gov法令検索
- 医薬品の製造販売後の調査及び試験の実施の基準に関する省令(GPSP省令)|e-Gov法令検索
- 臨床研究法|e-Gov法令検索
- 人を対象とする生命科学・医学系研究に関する倫理指針| 研究に関する指針について |厚生労働省



コメント