治験に参加を検討するとき、「副作用が怖い」と感じる方は少なくありません。でも実は、治験の世界には「副作用」と混同されやすい言葉がもう一つあります。それが「有害事象(AE)」です。
この2つは似ているようで、まったく異なる意味を持っています。そしてこの違いを理解することは、治験がいかに厳格な安全管理のもとで設計されているかを知ることに直結します。
元CRCとして患者さんのそばで3年間働き、現在はCRAとして治験全体を確認する立場から、できるだけ平易な言葉でお伝えします。
有害事象(AE)と副作用の違い
有害事象(Adverse Event / AE)とは?
治験薬を投与された患者さんに生じた、あらゆる好ましくない体調の変化や出来事のことです。
最も重要なポイントは、「治験薬との因果関係を問わない」という点です。治験中に起きたことであれば、薬のせいかどうかに関わらず、すべて「有害事象」として記録されます。
「この症状は、治験薬が原因で起きたのか」という関係性のことです。治験では、この因果関係が「あり」と判断されたものだけを「副作用」と呼びます。
副作用(Side Effect / Adverse Reaction)とは?
有害事象のうち、「治験薬との因果関係が否定できないもの」を指します。医師や専門家が「これは薬の影響によるものだ」と判断して、初めて「副作用」と呼ばれます。
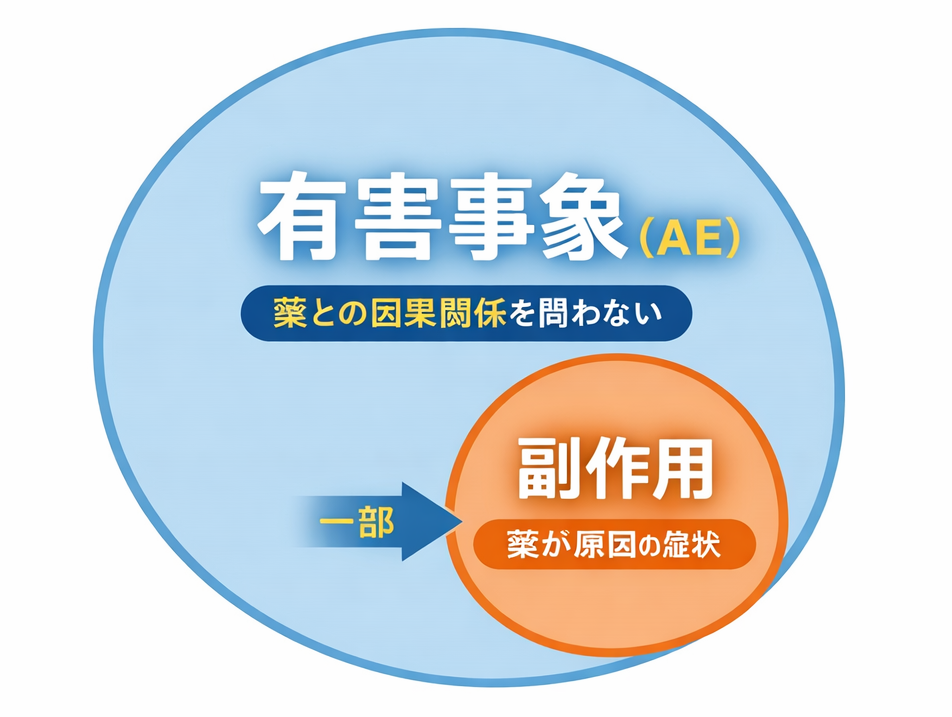
つまり、2つの関係はこのように整理できます。
有害事象(大きな網) ⊃ 副作用(その中の一部)
| 有害事象(AE) | 副作用 | |
|---|---|---|
| 対象 | 治験中のすべての好ましくない変化 | 薬との関係がある変化 |
| 因果関係 | 問わない | あり(または否定できない) |
| 報告の範囲 | 非常に広い | 有害事象の一部 |
⚖️根拠となる法令・ガイドライン 有害事象・副作用の定義は、ICH E2A(国際的なガイドライン)やGCP省令(医薬品の臨床試験の実施の基準に関する省令)に基づいています。
なぜ治験では「薬と関係ない出来事」まで報告するのか
「転んで骨折したのも報告が必要なんですか?」――現場でよく聞かれる質問です。答えは「はい、必要です」。
その理由は、治験の目的が「未知の情報を収集し、薬の安全性を客観的に評価すること」にあるからです。
たとえば、治験薬を服用中の患者さんが、雨の日に駅の階段で足を滑らせて骨折したとします。一見「雨で滑っただけ。薬とは無関係」に思えます。
しかし、世界中で同じ治験薬を飲んでいる患者さんから「転倒」や「ふらつき」の報告が相次いでいたとしたら?「単なる不注意」と思われていた出来事が、実は「薬によるわずかなめまい」が原因だった可能性が浮かび上がります。
一件一件は小さな点に見えても、集まることで初めて見える副作用がある。だからこそ、治験では因果関係を問わず、すべての変化を記録する仕組みになっているのです。
現場エピソード|皮膚科治験で見つけた「小さな変化」
CRCとして働いていた頃、皮膚科クリニックで塗り薬の治験を担当したことがあります。ほとんどの患者さんで元の疾患は改善傾向にあり、最も気にされていたかゆみも落ち着いていました。一見すると、順調な試験でした。
ただ、ある患者さんとの会話の中で気になることがありました。塗布部位に、毛穴詰まりのような黒いぽつぽつが目立っていたのです。本人は特に気にしておらず、私から指摘するまで意識していない様子でした。
「これは有害事象として拾うべきかもしれない」そう感じて、他の患者さんにも同様の症状がないかを確認していくと、同じ変化が複数人に続々と見つかりました。過去の試験成績には含まれていない情報でしたので、担当医と相談のうえ、製薬会社に直接報告・協議することになりました。
その後、その薬が市販された際、添付文書にそれらしき副作用情報が記載されていました。
患者さんが「特に気にしていなかった」小さな変化が、最終的に多くの人に届く情報として残ったのです。
「気になったら、まず拾う。」有害事象の報告とは、そういうことだと思っています。
重篤な有害事象(SAE)とは?その定義と範囲
同意説明文書(ICF)を読むと、「入院が必要になるような重い副作用」などの説明があり、不安に感じる方もいるかもしれません。こうした出来事は、治験では「重篤な有害事象」と呼ばれます。
ここで大切なのは、「重篤」という言葉の意味です。一般的な「重篤(重体)」とは少しニュアンスが違います。治験では、以下のいずれかに該当する出来事を「重篤な有害事象(SAE)」と呼びます。
- 死に至るもの
- 生命を脅かすもの
- 入院、または入院期間の延長が必要となるもの
- 永続的または顕著な障害・機能不全に陥るもの
- 先天異常を来すもの
たとえばがん治療の治験で、発熱により安全管理上1晩入院して経過を観察したケースも、定義上は「重篤な有害事象」に分類されます。日常生活の中で交通事故に遭ってしまったために入院。これも同じく重篤な有害事象になります。これらは「入院を要した」という事実が基準となるためで、必ずしも症状が深刻であることを意味せず、また治験薬との関係を問いません。
「重篤」という言葉を見て過度に不安になる必要はありません。これは「重大な変化の兆しを見逃さず、迅速に国や製薬会社へ報告し、安全性を再確認する」ための厳格な安全装置です。治験は、報告の仕組みが厳格であるほど、参加者が守られる設計になっています。
現場のプロは、それぞれどう関わっているのか
有害事象の管理は、一人の専門家が担うのではなく、複数の専門家がチームで支えています。
CRC(臨床研究コーディネーター)の役割
患者さんに最も近い存在であるCRCは、日常の何気ない会話から変化を察知します。
「最近、お変わりありませんか?」という問いかけに、「そういえば、少し食欲が落ちた気がする」と返ってきたとき――その言葉をこぼさず拾い上げ、医師に報告するのがCRCの役割です。患者さんの「主観的な変化」を「客観的なデータ」へと繋ぐ、橋渡し役と言えます。
担当医の役割
報告された有害事象に対し、医学的見地から因果関係を判定します。血液検査の結果・合併症の有無・薬を飲んでから症状が出るまでの時間などを総合的に判断し、「薬のせいか、それとも他の要因か」を判定します。
CRA(臨床開発モニター)の役割
病院から報告されたデータに漏れや矛盾がないかを確認します。カルテに記載された小さな体調の変化が、正しく有害事象として記録されているかをチェックし、治験全体のデータの信頼性を守ります。
治験参加中の患者さん・ご家族へ
治験に参加されている方、あるいはご家族を支えている方に、一つだけお伝えしたいことがあります。
「どんなに些細なことでも、隠さず伝えてください。」
「こんな小さなことを言ったら、治験が中止になってしまうのでは」「先生を煩わせてしまうのでは」――そう遠慮される方が、現場には少なくありません。
でも実際には逆です。些細な体調の変化を共有していただくことが、適切な処置を早めに行うことに繋がり、結果として患者さん自身を守ることになります。先ほどのエピソードのように、患者さんが「特に気にしていなかった」小さな変化が、後に多くの人を守る情報になることもあります。
治験は「新しい薬を試す場所」であると同時に、「徹底的に安全が守られるべき場所」でもあります。有害事象の報告は、その安全を守るための、最も基本的なステップです。気になったことがあれば、担当医やCRCに遠慮なく伝えてください。
まとめ
| 用語 | 意味 |
|---|---|
| 有害事象(AE) | 治験中に生じたあらゆる好ましくない変化(因果関係を問わない) |
| 副作用 | 有害事象のうち、薬との因果関係が否定できないもの |
| 重篤な有害事象(SAE) | 死亡・生命危機・入院・障害・先天異常のいずれかに該当するもの |
治験では、薬との因果関係を問わず、治験中のあらゆる好ましくない変化を「有害事象」として記録します。その中から科学的に薬との関係が認められたものが「副作用」と呼ばれます。一件一件は小さな点に見えても、集まることで初めて見えてくる副作用がある――だからこそ、すべてを記録する仕組みになっています。
「重篤な有害事象(SAE)」という言葉も、過度に恐れる必要はありません。どんな小さな変化も見逃さないための安全装置です。
治験に参加されている方へ――気になることは、どんなに小さくても伝えてください。その一言が、あなた自身を守り、未来の患者さんを守ることにつながっています。




コメント